- Detalhes
- Categoria: Coronavírus | covid-19
- By Fábio Reis
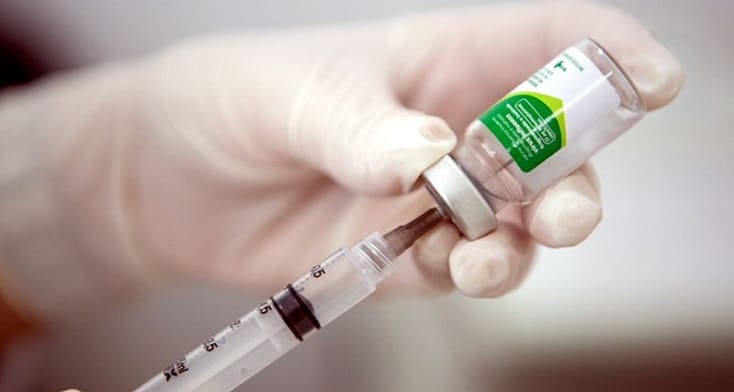
Confira o Plano de Monitoramento de Eventos Adversos de Vacinas:Documento inclui ações e estratégias específicas para Covid-19.
A Anvisa divulgou nesta sexta-feira (15/1) o Plano de Monitoramento de Eventos Adversos de Medicamentos e Vacinas Pós-Autorização de Uso Emergencial: Diretrizes e Estratégias de Farmacovigilância para o Enfrentamento da Covid-19, que reúne atividades já desenvolvidas pela área de Farmacovigilância da Agência em sua rotina, lições aprendidas com epidemias anteriores, na cooperação entre autoridades reguladoras de vários países do mundo, e estratégias específicas para monitorar os produtos destinados à pandemia de Covid-19.
O Plano de Monitoramento estabelece diretrizes e estratégias para apoiar a tomada de decisão regulatória em farmacovigilância durante a pandemia e se baseia no Sistema de Notificação e Investigação de Produtos em Vigilância Sanitária, no Programa Nacional de Imunização, nas Boas Práticas de Farmacovigilância e nas recomendações de organismos internacionais.
Grupos especializados
Entre as principais estratégias de monitoramento previstas no Plano, está a criação de uma sala de situação para a vigilância dos eventos adversos das vacinas contra Covid-19. É o chamado “MonitoraCovid-19”, que disponibilizará informações para subsidiar a tomada de decisão no âmbito regulatório, contribuindo para a transparência das ações de minimização ou interrupção dos possíveis riscos sanitários.
Fará parte do “MonitoraCovid-19” o Comitê Interno de Monitoramento de Produtos Pós-Autorização para a Covid-19, formado por servidores de áreas técnicas estratégicas da Agência para o acompanhamento dos dados de farmacovigilância, principalmente de vacinas e medicamentos. O objetivo aqui é identificar e facilitar o monitoramento dos eventos adversos, de forma a obter e dar respostas rápidas para aumentar a segurança da população.
Está sendo recriada a Câmara Técnica de Farmacovigilância, instituída pela primeira vez em 2017. Trata-se de um grupo constituído por especialistas com perfil técnico-científico de alto nível e que não fazem parte do corpo funcional da Anvisa. O propósito é assessorar a Agência na tomada de decisões regulatórias, nas pesquisas e formação de recursos humanos, na elaboração de relatórios e materiais técnico-científicos e na integração com instituições nacionais e internacionais, contribuindo para uma avaliação cuidadosa dos casos e garantindo julgamentos transparentes sobre a segurança das novas vacinas.
Tratamento das informações
Outro ponto a ser destacado é a integração dos sistemas VigiMed e e-SUS Notifica, que irá conferir maior robustez às análises de segurança e eficácia, bem como agilidade no envio das informações do monitoramento brasileiro à Organização Mundial da Saúde (OMS).
Vale lembrar que a Anvisa estabeleceu uma articulação estratégica com o Programa Nacional de Imunizações (PNI) para a vigilância epidemiológica e sanitária dos eventos adversos pós-vacinação. Isso inclui ações para o monitoramento dos vacinados, processos de investigação epidemiológica, avaliação dos casos e classificação de causalidade, por exemplo. Em outras palavras, as ações do PNI representam um braço importante para as ações de farmacovigilância das vacinas no setor público.
Outro aspecto relevante é o estímulo à comunicação dos eventos adversos ao sistema de saúde o mais rápido possível, tanto pelos profissionais de saúde, quanto pelo cidadão. O cidadão poderá contribuir reportando as suspeitas de eventos adversos o sistema VigiMed, agregando informações às estimativas de reações esperadas e não esperadas. Os dados registrados pelo cidadão estarão refletidos em relatórios, boletins ou alertas, conforme a relevância dos eventos reportados.
Em âmbito mundial, a Agência mantém canais regulares de comunicação com outras agências regulatórias e organizações internacionais de saúde. A troca rápida de informações sobre questões de segurança pode ocorrer por meio de alertas rápidos. Ademais, a Coalizão Internacional de Autoridades Reguladoras de Medicamentos (International Coalition of Medicines Regulatory Authorities – ICMRA) fornece uma estrutura para a troca de informações sobre iniciativas e melhores práticas relacionadas às emergências de saúde pública e à Covid-19.
Observa-se ainda que a Anvisa trabalhará com redes de colaboradores, fabricantes e profissionais de saúde, e divulgará todas as informações relevantes sobre as vacinas contra a Covid-19 para sua rede e no portal eletrônico do Governo Federal.
Qualificação
Outra ação importante a fim de se obter um monitoramento de segurança e qualidade adequado à gestão das vacinas contra Covid-19 é o preparo das equipes de vigilância. Para apoiar e reforçar o conhecimento necessário, a Anvisa e o Ministério da Saúde vêm promovendo reuniões com as coordenações estaduais de imunizações para apresentação do Protocolo de Vigilância de Eventos Adversos para Covid-19 e dos respectivos fluxos já definidos. A intenção é orientar as secretarias de saúde e os profissionais sobre a vigilância das pessoas vacinadas e sobre a vacina.
Parcerias
As parcerias são imprescindíveis para a formação de um sistema de farmacovigilância coeso, forte e eficiente. A colaboração de todos os envolvidos não é somente estratégica, mas essencial. Nesse sentido, cumpre destacar a dobradinha da Anvisa com a Secretaria de Vigilância em Saúde (SVS) do Ministério da Saúde para avaliação tempestiva de casos de eventos adversos e intervenção oportuna.
Por fim, é importante destacar que o Plano de Monitoramento deverá ser aperfeiçoado sempre que necessário, conforme necessidades regulatórias e/ou surgimento de novos conhecimentos técnico-científicos que demandem a atualização de ações e estratégias para minimização de riscos.
Conheça as diretrizes e as estratégias dispostas no Plano de Monitoramento de Eventos Adversos de Medicamentos e Vacinas Pós-Autorização de Uso Emergencial: Diretrizes e Estratégias de Farmacovigilância para o enfrentamento da Covid-19.













