- Detalhes
- Categoria: Coronavírus | covid-19
- By Jornal da USP

Texto por Arthur Gruber, professor do Departamento de Parasitologia do Instituto de Ciências Biomédicas da USP
Coronavírus - Vírus da família Coronaviridae causam uma variedade de doenças no homem e nos animais, especialmente no trato respiratório. As partículas virais são esféricas, com cerca de 125 nm de diâmetro e revestidas por um envelope fosfolipídico. O genoma de RNA de fita simples e senso positivo contém entre 26 a 32 quilobases e está associado a proteínas, formando o nucleocapsídeo. As partículas apresentam projeções que emanam do envelope em forma de espículas, formadas por trímeros da proteína S (spike protein). Essas projeções geram um aspecto de coroa, daí a denominação coronavírus. A proteína S é responsável pela adesão do vírus nas células do hospedeiro e participa do processo de interiorização, no qual ocorre a fusão entre as membranas viral e da célula e a entrada do vírus no citoplasma.
No caso do Sars-CoV-2, causador da atual pandemia de covid-19, a proteína S reconhece através de seu domínio ligante do receptor (RBD) o receptor ACE2 (enzima conversora de angiotensina 2) da célula. Sete espécies podem infectar humanos, sendo que três podem produzir doenças graves, o Sars-CoV-2, o Sars-CoV, agente da pandemia de Sars (síndrome respiratória aguda grave) de 2002-2003 e o Mers-CoV, causador da Mers (síndrome respiratória do Oriente Médio). Os coronavírus HKU1, NL63, OC43 e 229E estão associados a doenças com sintomatologia leve.
Leia também: Coronavírus SARS-CoV-2 não é um vírus feito em laboratório
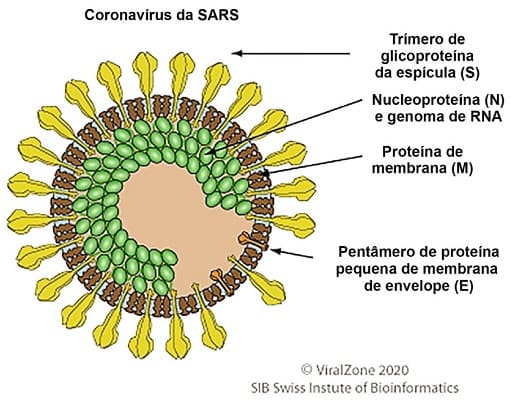
Estrutura de uma partícula viral de um coronavírus – Imagem: ViralZone
Os primeiros relatos
O primeiro caso oficial de covid-19 (coronavirus disease 2019) foi de um paciente hospitalizado no dia 12 de dezembro de 2019 em Wuhan, China, mas estudos retrospectivos detectaram um caso clínico com sintomas da doença em 01/12/19. O primeiro artigo científico, publicado algumas semanas depois por pesquisadores chineses, descreveu o caso de um paciente de 41 anos admitido no Hospital Central de Wuhan em 26 de dezembro. O fluido broncoalveolar continha um vírus cujo genoma mostrou uma relação filogenética com coronavírus causadores da Sars e Mers. O vírus, denominado WHCV (posteriormente 2019-nCoV e finalmente Sars-CoV-2), mostrou alta similaridade genômica com o Bat SL-CoVZC45, um vírus obtido de um morcego coletado na China. Esse resultado sugeriu que esse novo coronavírus poderia ter se originado de morcegos, um reservatório já identificado para o Sars-CoV, agente da Sars.
Quando surgiu o Sars-CoV-2?
Várias evidências excluem a hipótese de que o Sars-CoV-2 tenha tido uma origem laboratorial. No caso da Sars, sabe-se que o vírus foi transmitido de morcegos para civetas e desses hospedeiros intermediários para o homem, mas para o Sars-CoV-2 essa questão permanece em aberto. Em dezembro de 2019, iniciou-se um surto que atingiu cerca de 50 pessoas na cidade de Wuhan, na China. A maioria dos pacientes tinha sido exposta ao mercado Huanan. Esse mercado comercializava frutos do mar, mas também animais silvestres, frequentemente vendidos vivos ou abatidos no local. Contudo, vários pacientes desse surto inicial não tiveram relação epidemiológica com o mercado, abrindo a possibilidade de que outras fontes de infecção pudessem estar envolvidas.
Um estudo estimou o tempo do ancestral comum mais recente (TMRCA) para metade e o final de novembro de 2019. Outro grupo de pesquisa obteve um tempo parecido, entre 22 a 24 de novembro de 2019. Esse período em que um vírus ancestral de todos os isolados Sars-CoV-2 poderia ter surgido é próximo do dia primeiro de dezembro, data na qual o primeiro caso clínico com sintomas da covid-19 foi relatado.
Qual é a origem do Sars-CoV-2?
Ao lado de vírus encontrados em morcegos, vários artigos relataram a presença de coronavírus em pangolins, com similaridade de 85,5-92,4% com o genoma do Sars-Cov-2. Pangolins são vendidos ilegalmente na China pela sua carne, escamas e uso na tradicional medicina chinesa. Embora em princípio não fossem vendidos no mercado de Wuhan, não é possível descartar a sua possível venda ilegal.
O genoma do Sars-CoV-2 apresenta 96% de similaridade com o do vírus RaTG13, obtido do morcego Rhinolophus affinis, valor bastante superior à similaridade observada com vírus de pangolins, o que sugere que o pangolim não tenha transmitido o vírus diretamente ao homem. O RBD do SARS-CoV-2 é capaz de aderir com alta afinidade no receptor ACE2 humano, mas, dos seis resíduos de aminoácidos identificados como essenciais para a ligação, somente um é compartilhado com o Sars-CoV, causador da Sars, ou com o RaTG13. Isso indica que o Sars-CoV-2 desenvolveu através da seleção natural um novo sítio otimizado para a interação com o receptor humano. Por outro lado, vírus de pangolins, apesar de terem menor semelhança genômica com o Sars-CoV-2 do que vírus de morcego, apresentam uma região RBD muito mais parecida, conservando cinco dos seis resíduos de aminoácidos essenciais para a interação.
Segundo Alexandre Hassanin, pesquisador da Universidade de Sorbonne, é possível que o vírus transmitido a humanos tenha sido um produto quimérico resultante da recombinação entre um vírus próximo ao RaTG12 de morcego e um segundo vírus próximo do vírus de pangolim. Portanto, parece faltar um elo perdido que possa explicar a origem do Sars-CoV-2.
Outra descoberta interessante é a existência de uma inserção de uma sequência polibásica antecedida por uma prolina (resíduos PRRAR) na junção das porções S1 e S2 da proteína S. Essa região pode estar envolvida na clivagem por furina e outras proteases do hospedeiro e ter implicações na transmissibilidade do vírus e na definição da especificidade de seus hospedeiros. O sítio de clivagem é encontrado no Sars-CoV-2, mas não nos coronavírus de morcegos e pangolins.
Segundo as revisões de Andersen e colaboradores, e Zhang e Holmes, para que um vírus precursor adquirisse por um processo evolutivo os sítios RBD de alta afinidade e de clivagem por proteases, seria necessária a sua passagem por um hospedeiro intermediário com alta densidade populacional, que tivesse uma proteína ACE2 semelhante à humana. Após a aquisição dessas características, o vírus teria se transferido para o homem. Alternativamente, o vírus progenitor do SARS-CoV-2 poderia ter adquirido o sítio polibásico após a transferência zoonótica. Assim, o vírus teria se multiplicado em humanos de forma críptica sem causar sintomatologia grave e, após a aquisição dessa característica, teria aumentado sua transmissibilidade e patogenicidade, desencadeando assim a covid-19. Segundo David Robertson, pesquisador da Universidade de Glasgow, “o hospedeiro intermediário é a peça que falta no quebra-cabeça: como todas essas pessoas se infectaram?”.
Um modelo experimental e a busca pelo hospedeiro intermediário
Em um artigo recente, pesquisadores chineses fizeram análises de modelagem estrutural e de interação entre o sítio RBD da proteína S e o receptor ACE2 e observaram que o hamster, dentre as diferentes espécies de animais de experimentação testadas, apresenta a maior afinidade entre as duas proteínas. Infecções experimentais reproduziram as principais manifestações clínicas e lesões da covid-19, validando seu uso como modelo de infecção experimental.
Estudos de afinidade entre o sítio RBD e ACE2 de diferentes espécies animais têm sido feitos, visando identificar potenciais candidatos a hospedeiros intermediários. Os candidatos seriam possivelmente uma ou mais espécies de animais presentes em mercados chineses, sendo que desses, um dos mais próximos do hamster é o rato de bambu. Esse animal é encontrado em vários países asiáticos, incluindo as regiões central e sudeste da China. Muito populares na culinária chinesa, os ratos de bambu são capturados nos seus habitats naturais ou criados em larga escala em fazendas. Recentemente, Zhong Nanshan, médico chinês que conduziu os esforços contra a Sars entre 2003 e 2004 e lidera o grupo de especialistas contra a covid-19, apontou em entrevista que o rato de bambu é um provável hospedeiro intermediário do Sars-CoV-2. O pesquisador embasou sua hipótese no fato que o arquipélago de Zhoushan, localizado no leste da China, é o habitat natural de ratos de bambu, morcegos e pangolins, o que teria possibilitado a transmissão viral entre esses hospedeiros antes de sua passagem para o homem.
Para validar essa hipótese, seria necessário se avaliar a afinidade da ACE2 de ratos de bambu com a proteína S viral, realizar infecções experimentais, avaliar as manifestações clínicas e patológicas e testar a capacidade de transmissão viral entre indivíduos. Caso a suscetibilidade de infecção dessa espécie venha a ser comprovada, levantamentos metagenômicos poderiam estabelecer seu papel na transmissão do Sars-CoV-2 para humanos. Será que finalmente encontraremos o elo perdido que falta no quebra-cabeça da origem e transmissão do Sars-CoV-2?
Texto por Arthur Gruber
Fonte: Jornal da USP













