- Detalhes
- Categoria: Coronavírus | covid-19
- By Fábio Reis
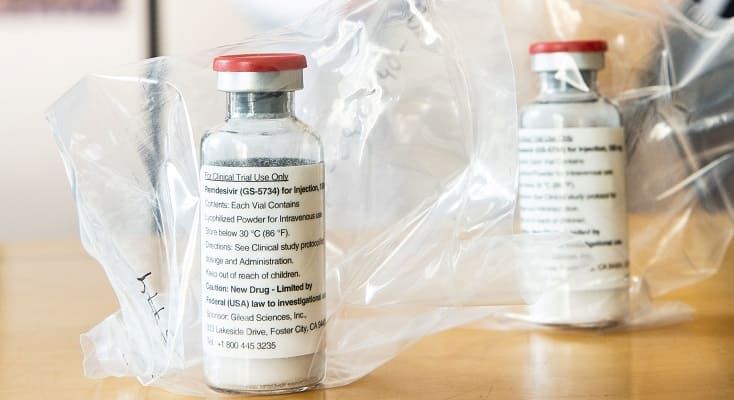
O Remdesivir (GS-5734 ™) é um medicamento antiviral desenvolvido por Gilead Sciences desenvolvido inicialmente para tratamento do Ebola, mas experimental para para tratamento de doenças como MERS e em fase de testes para o novo coronavírus SARS-CoV-2.
Remdesivir está autorizado para o tratamento de pacientes hospitalizados em estado grave da doença COVID-19. Ele está autorizado para pacientes adultos ou pediátricos internados em um hospital e para os quais o uso de um agente intravenoso seja clinicamente apropriado, pois o remdesivir deve ser administrado por via intravenosa.
A duração ideal do tratamento ainda está sendo estudada em ensaios clínicos em andamento. Nos EUA, sugerem-se durações de tratamento de 5 a 10 dias, com base na gravidade da doença.
No dia 1º de maio o remdesivir recebeu autorização de uso de emergência da FDA. A Autorização permite uso mais amplo. A autorização é temporária e não substitui o processo formal de envio, revisão e aprovação de novos medicamentos. O medicamento continua sendo um medicamento experimental e não foi aprovado pelo FDA.
Os EUA baseiam-se nos dados disponíveis de dois ensaios clínicos globais - o estudo de Fase 3, controlado por placebo, do Instituto Nacional de Alergias e Doenças Infecciosas, em pacientes com sintomas moderados a graves de COVID-19, incluindo aqueles que estavam gravemente enfermos, e o estudo mundial da Gilead.
O Estudo de fase 3 que avaliou as durações de 5 e 10 dias da dose de remdesivir em pacientes com doença grave. Vários ensaios clínicos adicionais estão em andamento para gerar mais dados sobre a segurança e a eficácia do remdesivir como tratamento para o COVID-19.
A empresa destaca que existem dados clínicos limitados disponíveis para o remdesivir. Podem ocorrer eventos adversos graves e inesperados que não foram relatados anteriormente com o uso do remdesivir.
Em estudos clínicos com remdesivir, foram observadas reações relacionadas à infusão e elevação das transaminases hepáticas. O remdesivir não deve ser utilizado em pacientes hipersensíveis a qualquer ingrediente do remdesivir.
Os pacientes devem ter monitoramento clínico e laboratorial adequado para ajudar na detecção precoce de possíveis eventos adversos. Monitorar a função renal e hepática antes de iniciar e diariamente durante o tratamento com remdesivir. Deve-se monitorar o nível sérico diariamente durante o tratamento.
Em fevereiro a farmacêutica chinesa BrightGene Bio-Medical Technology disse que começou a produzir em larga escala o medicamento experimental da Gilead Sciences.
O medicamento não está autorizado para o tratamento de outros vírus ou patógenos.
A Gilead Sciences é uma empresa biofarmacêutica que descobre, desenvolve e comercializa terapias inovadoras em áreas com necessidades médicas não atendidas.
Texto por Fábio Reis para PFARMA
* A reprodução é permitida desde que citada a fonte com link para https://pfarma.com.br
Sobre Estudos Clínicos de medicamentos experimentais para combater o coronavírus:
- Estudo in vitro com Ivermectina
- Hidroxicloroquina apresenta bons resultados contra o coronavírus
- Sobre o uso do Ibuprofeno, Cortisona e Tiazolidinediona em infecções por Coronavírus
- Takeda está desenvolvendo terapia derivada do plasma para o coronavírus
- Favipiravir demonstra eficácia no tratamento do Coronavírus













